近日,暨南大学物理与光电工程学院关柏鸥教授团队利用双等离子界面功能化的微纳光纤生物传感器,实现了肿瘤的检测和光热治疗。该成果以“Marriage of a Dual-Plasmonic Interface and Optical Microfiber for NIR-II Cancer Theranostics”为题发表在Advanced Materials第36卷第8期上。关柏鸥教授、黄赟赟研究员为共同通讯作者,暨南大学博士研究生吴昊天、博士后陈鹏伟为论文的共同第一作者,该工作由暨南大学独立完成。

对于致死率高居全球首位的癌症,早期的诊断和治疗是提升治愈率和生存率的关键。传统的手术、化疗和放疗,是目前大多数癌症患者可用的临床治疗方法。但是由于不可避免的耐药和耐辐射,传统的化疗和放疗疗效较差。光一直是一种治疗疾病的有效方式。随着光子学和光学技术的革命性进步,光开辟了肿瘤治疗的新时代,为基于光的肿瘤治疗提供了丰富的自由度。光热疗法(photothermal therapy, PTT)作为一种新兴的以光为介质的癌症治疗方法,利用纳米材料吸收光子中的能量,并将其部分以热的形式耗散,从而引发癌细胞的死亡,因其无创性、特异性和效率高、副作用小等特点而备受关注。近年来,光热材料迅猛发展,有力地推动了光热治疗技术的发展和应用。然而,作为一种利用光作为激励源的治疗工具,光热治疗仍然面临着两大主要的挑战:光在体内的穿透深度有限,光热材料在正常组织的非特异性聚集和伤害问题。
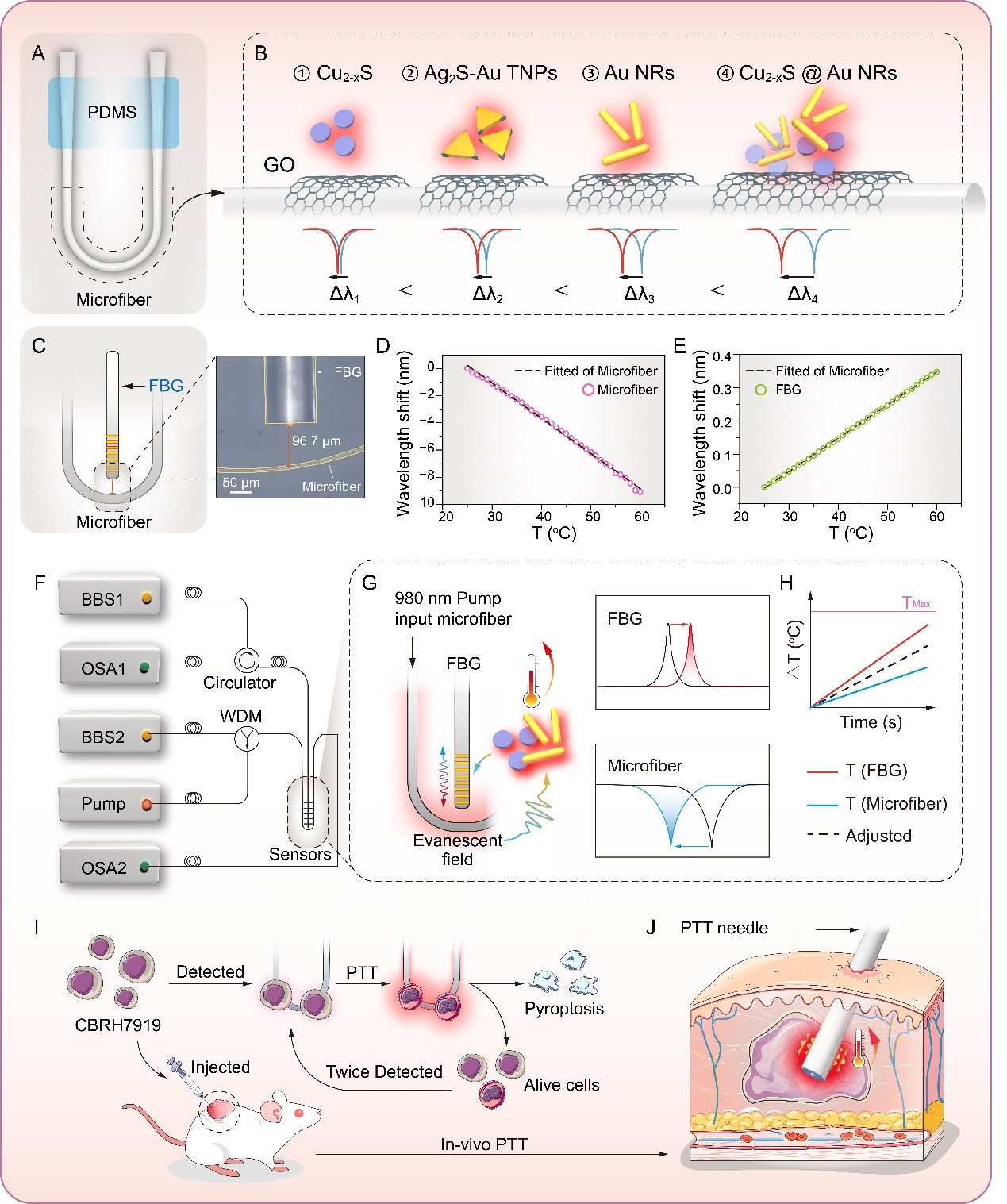
光纤提供了解决上述问题的可能性。光纤作为生物传感器已广泛应用于疾病标志物检测领域。而在光热治疗领域,光纤可以在体内作为光引导介质,从而大大减少光在组织中的散射和吸收,克服光穿透深度有限的障碍;光热剂也可以集成在光纤表面,以解决光热剂在正常组织的积累和伤害问题。在前期工作的基础上,关柏鸥教授、黄赟赟研究员团队提出了一种通过界面设计将光纤和光热剂相结合的设计理念,实现了集癌症检测和治疗功能于一体的光热诊疗纤维。该纤维由金纳米棒和硫化铜双等离子体纳米界面和微纳光纤组成,双等离子界面通过局域表面等离子共振效应增强光纤倏逝场,从而提升传感器灵敏度,同时,界面具有较高的光热转化效率(78.9%),可以利用很低的泵浦功率对传感器界面温度进行自由调节,用于自热检测和肿瘤消融。利用双等离子界面的增敏效应和光热效应,并在界面上组装识别分子层,可用于区分癌细胞和正常细胞,量化癌细胞,对癌细胞进行超热消融,并评估消融效果。该传感器作为治疗深部肿瘤的独特工具具有很大的前景,并为探索紧凑的光治疗设备提供了有前途的策略。双等离子体纳米界面和微纳光纤的结合代表了一种新的光热治疗概念,具有克服有限的光穿透深度和光敏剂非特异性积累以及对正常组织的意外伤害的潜力。该器件有望实现癌症诊断、治疗和术后监测的同步进行,加快智能治疗的开发和临床转化。
该工作得到国家自然科学基金(62375108,U1701268)、广东特支计划本土团队项目(2019BT02X105)、广东省自然科学基金(2019A1515011278)、广州市市校联合基金(2023A03J0130)等项目的资助。
论文链接:https://onlinelibrary.wiley.com/doi/full/10.1002/adma.202310571
图文:黄赟赟
校对:杨嘉琳
责任编辑:邓玉萌
初审:肖艳芳
复审:孙玉环
终审发布:黄睿
